Sıhhat Bakanı Fahrettin Koca, TURKOVAC için dün acil kullanım onayı müracaatının yapıldığını, aşının yıl bitmeden yaygın kullanıma girmesinin ümit edildiğini açıkladı.
Edinilen bilgiye nazaran, Türkiye İlaç ve Tıbbi Aygıt Kurumuna (TİTCK) yapılan bu müracaat sonrasında, TURKOVAC’ın acil kullanım onayını alması en az 3 haftalık süreci gerektirecek.
Bu sürecin olumlu sonuçlanması durumunda aşının seri üretimine geçilecek. Sıhhat Bakanlığı, TURKOVAC’ın seri üretiminin Türkiye’de iki tesiste yürütülmesini planlıyor.
AA muhabiri, Türkiye’nin “kendi aşısını üreten ülke” olarak salgınla çabada elini güçlendirmesi ve aşıyı tüm insanlığın kullanımına sunması açısından da büyük kıymet taşıyan TURKOVAC’ın bugüne kadar geçirdiği süreçleri 5 unsurda derledi.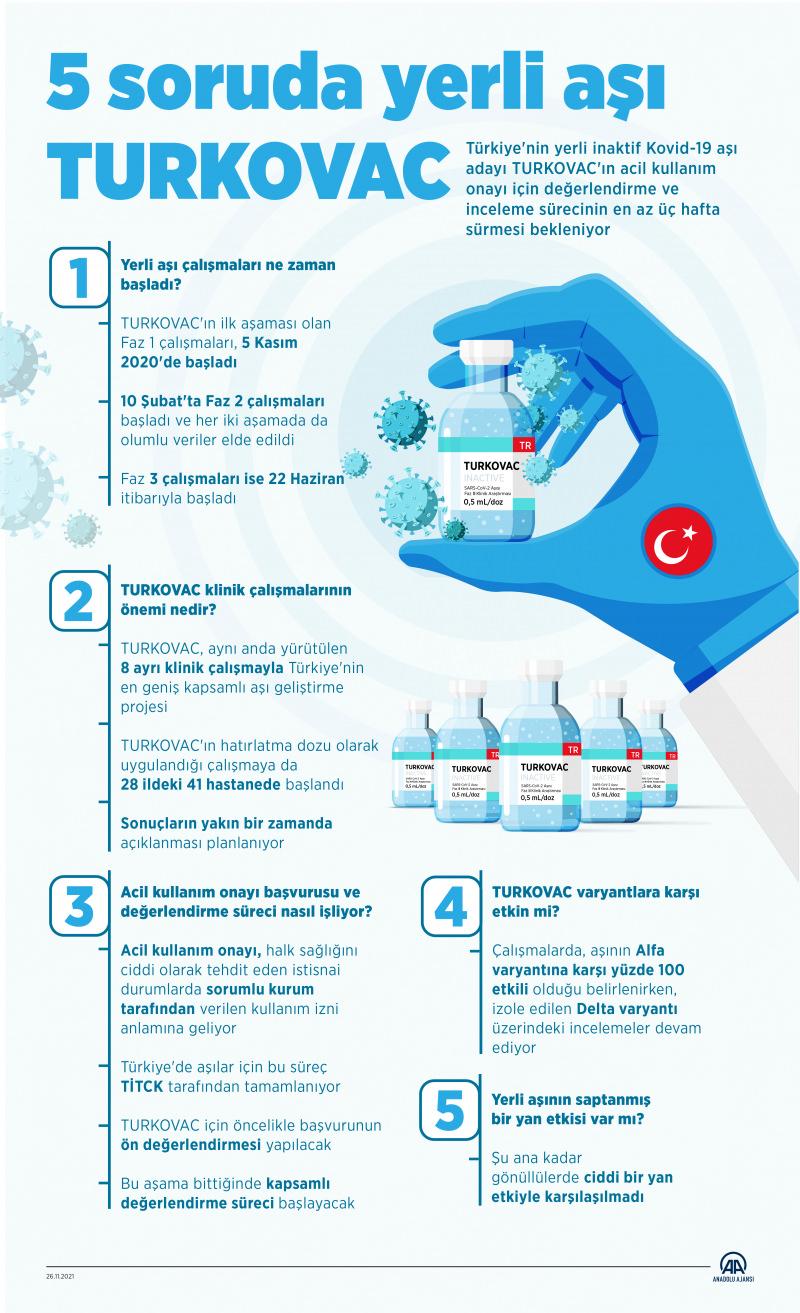
1- Yerli aşı çalışmaları ne vakit başladı?
Erciyes Üniversitesi ve Sıhhat Bakanlığı Türkiye Sıhhat Enstitüleri Başkanlığı (TÜSEB) iş birliğiyle geliştirilen TURKOVAC’ın birinci kademesi olan Faz 1 çalışmaları, 5 Kasım 2020’de başladı.
44 istekli üzerinde uygulanan Faz 1 kademesinin akabinde birinci dozu 10 Şubat’ta yapılan Faz 2 çalışmaları ise 250 gönüllüyle yürütüldü ve her iki kademede da aşıyla ilgili olumlu datalar elde edildi.
Yerli aşının aktifliğinin daha geniş bir kitle üzerinde değerlendirilmesini içeren Faz 3 çalışmaları ise 22 Haziran prestijiyle başladı. Yurt içi ve dışında binlerce gönüllünün iştirakiyle yürütülen Faz 3 çalışmaları kapsamında daha evvel koronavirüs geçirmeyen ve hiç Kovid-19 aşısı olmayanlara TURKOVAC’ın uygulanmasına devam ediliyor.
2- TURKOVAC klinik çalışmalarının değeri nedir?
TURKOVAC, tıpkı anda yürütülen 8 başka klinik çalışmayla Türkiye’nin en geniş kapsamlı aşı geliştirme projesi olma özelliği taşıyor.
Klinik çalışmalar kapsamında en son ekim ayında TURKOVAC’ın hatırlatma dozu olarak uygulandığı çalışmaya 28 vilayetteki 41 hastanede başlandı.
Hatırlatma dozu çalışması kapsamında, daha evvel Kovid-19 geçirmemiş ve 2 doz Sinovac aşısı olmuş, 18-59 yaş ortası sağlıklı bireyler ortasından seçilen gönüllülerin yarısına üçüncü doz olarak TURKOVAC, öbür yarısına da Sinovac aşısı uygulandı.
TÜSEB takviyesi ile yürütülen bu klinik çalışma tamamlanma etabına geldi. Sonuçların yakın bir vakitte açıklanması planlanıyor.
3- Acil kullanım onayı başvurusu ve kıymetlendirme süreci nasıl işliyor?
Acil kullanım onayı, Dünya Sıhhat Örgütü yahut Sıhhat Bakanlığı tarafından bulaşıcı hastalıklar kapsamında kabul edilen, halk sıhhatini önemli olarak tehdit eden istisnai durumlarda sorumlu kurum tarafından verilen kullanım müsaadesi manasına geliyor.
Türkiye’de aşılar için bu süreç, TİTCK tarafından “Acil Kullanım Onayı Başvurusu ve Değerlendirmesi Hakkında Kılavuz” ışığında yürütülen incelemeler sonucunda tamamlanıyor.
Buna nazaran, yerli aşı adayı TURKOVAC için öncelikle müracaatın ön değerlendirmesi yapılacak. Bu kademe bittiğinde ise aşıyla ilgili yürütülen çalışmaların sonuçlarına odaklanılacak ve kapsamlı kıymetlendirme süreci başlayacak.
Kıymetlendirme evresinde aşının yarar/risk istikrarı, klinik dataları, halk sıhhatine yararları üzere kıstaslar bilimsel ve milletlerarası standartlara nazaran ele alınacak.
4- TURKOVAC varyantlara karşı aktif mi?
Yerli aşı adayı TURKOVAC’ın çeşitli varyantlar üzerinde aktifliğine yönelik çalışmalar da yürütülüyor.
Bu çerçevede aşının Alfa varyantına karşı yüzde 100 tesirli olduğu belirlenirken, izole edilen Delta varyantı üzerindeki incelemeler devam ediyor.
5- Yerli aşının saptanmış bir yan tesiri var mı?
Dünyada aşı çalışmaları için belirlenmiş standartlar olan GLP, GMP ve GCP standartlarına uygun formda yürütülen TURKOVAC inaktif aşı geliştirme çalışmalarında, şu ana kadar gönüllülerde önemli bir yan tesirle karşılaşılmadı.